L’impiego della Deep Brain Stimulation (DBS) in Neurologia è storicamente associato al trattamento dei disturbi del movimento (ad es. malattia di Parkinson, tremore essenziale, distonie). Meno noto è invece il suo utilizzo nell’ambito dell’epilessia.
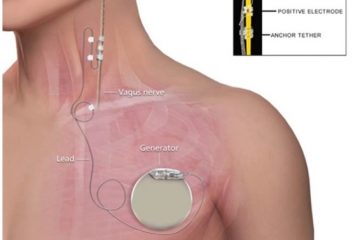
Nel mondo, circa 50 milioni di persone soffrono di epilessia e di queste circa il 20% è farmacoresistente. Secondo la definizione della ILAE (International League Against Epilepsy) con “farmacoresistenza” si intende il mancato controllo delle crisi nonostante l’assunzione di due farmaci antiepilettici diversi, appropriati per il tipo di epilessia, in monoterapia o in associazione. In questi pazienti, la prima linea di trattamento da prendere in considerazione è la chirurgia resettiva. Tuttavia, in coloro i quali la chirurgia è controindicata o inefficace, un’altra opzione terapeutica da prendere in considerazione è la DBS che consiste nella stimolazione elettrica di strutture cerebrali profonde attraverso l’impianto di elettrodi connessi con dei generatori di impulsi. Le prime evidenze di un beneficio della DBS nella riduzione della frequenza critica risalgono agli anni ’70-80. Ad oggi comunque i meccanismi pato-fisiologici sottesi a questa metodica di stimolazione non sono ancora completamente conosciuti, tanto che alcuni pazienti risultano beneficiare dalla DBS mentre altri no, ma le ragioni ancora non sono del tutto note.
Per questi motivi ad oggi la principale indicazione alla DBS risulta essere la presenza di una epilessia farmacoresistente in cui la chirurgia resettiva sia controindicata (ad esempio attività epilettica diffusa, focus epilettico in prossimità di importanti aree funzionali, mancanza di alterazioni al neuroimaging, basso rischio operatorio nell’impianto degli elettrodi rispetto all’intervento chirurgico resettivo). In sostanza, l’impiego della DBS in questi pazienti avrebbe ancora un intento palliativo e non curativo, anche se nei pazienti “responders” permetterebbe un netto miglioramento della qualità della vita e dell’aspetto cognitivo, oltre a una riduzione della terapia farmacologia. Gli effetti collaterali sarebbero i medesimi riportati nell’impianto nei pazienti con disturbi del movimento (ad esempio infezioni, dislocamento degli elettrodi, algie o parestesie legate alla stimolazione, emorragie).
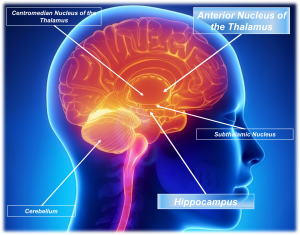
Quali risultano essere quindi le strutture cerebrali target della DBS nell’epilessia? Le migliori evidenze riguardano la stimolazione del nucleo anteriore del talamo e dell’ippocampo. L’efficacia della stimolazione di altre strutture cerebrali è ad oggi inconclusiva per mancanza di sufficiente evidenza scientifica.
Il nucleo anteriore del talamo (NA) è coinvolto nel circuito di Papez e collega l’ippocampo al fornice attraverso il fascio mammillotalamico, prima delle proiezioni diffuse alla corteccia del cingolo e alla neocorteccia. Risulta quindi intuitivo comprendere come la stimolazione di NA possa impedire la secondaria generalizzazione di scariche epilettiche ad esordio focale. Lo studio più grande al riguardo è lo studio SANTE pubblicato nel 2010 che ha coinvolto 110 pazienti con epilessie focali, con e senza secondaria generalizzazione. I pazienti con epilessia del lobo temporale sono risultati quelli che hanno riportato maggior beneficio (miglioramento della frequenza critica del 44% a 1 anno e del 76% a 5 anni). Come possibili effetti avversi sono stati segnalati depressione e disturbi di memoria, evidenti se si pensa al ruolo di tale circuito negli aspetti emozionali e della memoria.
La stimolazione dell’ippocampo è anch’essa legata al suo ruolo nel circuito di Papez. I pazienti in cui sono stati ottenuti i migliori risultati sono stati quelli con epilessia del lobo temporale mesiale, soprattutto senza associata evidenza di sclerosi ippocampale alla RMN.
Altre sedi di stimolazione studiate sono state il nucleo centromediano del talamo (soprattutto in pazienti con sindrome di Lennox-Gastaut ed epilessie generalizzate), cervelletto e nucleo subtalamico, ma solo su un numero esiguo di pazienti e quindi, come detto sopra, con risultati non univoci.
Chiara Pizzamiglio, Novara
Bibliografia:
1) Sprengers M, Vonck K, Carrette E, Marson AG, Boon P. Deep brain and cortical stimulation for epilepsy. Cochrane Database Syst Rev. 2017 Jul 18;7. doi: 10.1002/14651858.CD008497.pub3.
2) Bouwens van der Vlis TAM, Schijns OEMG, Schaper FLWVJ, Hoogland G, Kubben P, Wagner L, Rouhl R, Temel Y, Ackermans L. Deep brain stimulation of the anterior nucleus of the thalamus for drug-resistant epilepsy. Neurosurg Rev. 2018 Jan 6. doi: 10.1007/s10143-017-0941-x.
3) Fisher R, Salanova V, Witt T, Worth R, Henry T, Gross R, et al., Electrical stimulation of the anterior nucleus of thalamus for treatment of refractory epilepsy. SANTE Study Group. Epilepsia. 2010 May;51(5):899-908. doi: 10.1111/j.1528-1167.2010.02536.x.
4)Oh Y-S, Kim HJ, Lee KJ, et al. Cognitive improvement after long-term electrical stimulation of bilateral anterior thalamic nucleus in refractory epilepsy patients. Seizure. 2012;21:183–7. doi: 10.1016/j.seizure.2011.12.003.
5)Velasco AL, Velasco F, Velasco M, et al. The role of neuromodulation of the hippocampus in the treatment of intractable complex partial seizures of the temporal lobe. Acta Neurochir Suppl. 2007;97:329–32. PMID: 17691319.