L’epilessia è tra i disturbi neurologici cronici più comuni e interessa circa 50 milioni di persone in tutto il mondo. Nonostante l’esistenza di oltre 20 farmaci anticrisi, circa 15 milioni di pazienti risultano resistenti alla terapia farmacologica. La Lega Internazionale contro l’Epilessia (ILAE) definisce farmacoresistente un paziente in cui si sia verificato il fallimento di almeno due farmaci anticrisi nonostante l’uso appropriato degli stessi, somministrati in monoterapia o in combinazione e scelti in modo adeguato al tipo di epilessia o sindrome epilettica del paziente. In tale contesto, un valido aiuto nella gestione delle epilessie farmacoresistenti è rappresentato dalle terapie non farmacologiche, che consentono di minimizzare la quantità di farmaci assunti dai pazienti e di conseguenza di ridurre al minimo gli eventuali effetti collaterali.
La VNS (dall’inglese, Vagus Nerve Stimulation) rappresenta un’opzione terapeutica per i pazienti farmacoresistenti che risultano non candidabili a interventi chirurgici risolutivi o che scelgono di non sottoporsi a tali procedure (circa il 40% dei pazienti farmacoresistenti).
Il VNS è, in effetti, un dispositivo con una lunga storia alle spalle. La prima pubblicazione risale al 1938; nel 1994 ha ricevuto l’approvazione dell’Unione Europea e tre anni dopo è stato approvato dalla Food and Drug Administration come trattamento aggiuntivo nei casi di epilessia farmacoresistente in adulti e adolescenti sopra i 12 anni di età. Nel 2017, l’indicazione per la stimolazione del nervo vago (VNS) è stata estesa anche ai bambini di età superiore ai 4 anni. Questo ampliamento è stato motivato dall’evidenza che un intervento precoce offre risultati migliori, in particolare nelle forme di epilessia grave, come quelle associate a sindromi genetiche.
Il dispositivo VNS consiste in un generatore di impulsi, un sistema di elettrodi impiantati attorno al nervo vago e un programmatore esterno che si utilizza per il settaggio della stimolazione. Il generatore di impulsi è un dispositivo multi-programmabile che eroga corrente elettrica al nervo vago, ed è allocato in un contenitore ermetico al titanio, alimentato da una batteria. Gli impulsi elettrici sono trasmessi dal generatore al nervo vago tramite gli elettrodi. Questi ultimi ed il generatore costituiscono la parte impiantabile del sistema VNS, che viene impiantato sottocute in regione sottoclaveare sinistra.
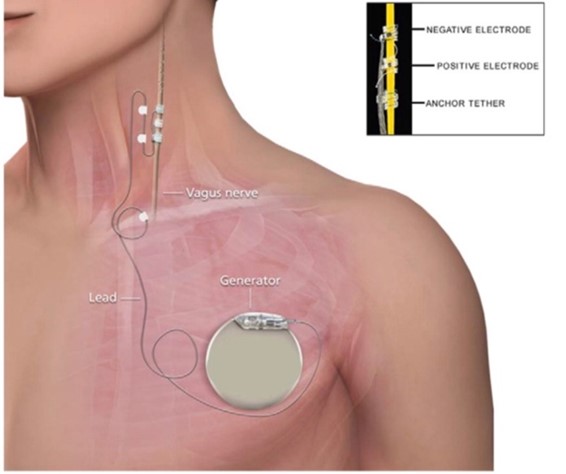
Il sistema di programmazione esterno comprende un dispositivo programmabile, il software di programmazione e un computer compatibile. Il software consente al medico, tramite il dispositivo programmabile posizionato sul generatore di impulsi, di identificare e modificare le impostazioni del dispositivo.

Riguardo il suo funzionamento, l’elettrodo negativo genera potenziali d’azione i quali si muovono in direzione afferente attraverso le fibre sensoriali del nervo vago e vengono in larga misura bloccati da un elettrodo positivo; gli impulsi che non vengono bloccati possono essere alla base degli effetti collaterali del VNS: tosse, raucedine, dolore al collo e disturbi del sonno. Tipicamente, però, questi disturbi sono transitori, tendono a ridursi con il protrarsi della terapia e possono comunque essere ridotti o eliminati regolando le impostazioni dei parametri del dispositivo. Dal punto di vista delle complicanze chirurgiche, invece, la più comune è l’infezione del sito di impianto, che può comunque essere facilmente gestita con antibiotici.
La VNS tradizionale prevede due modalità di stimolazione: la modalità normale (ad anello aperto) e la modalità magnetica (su richiesta). La stimolazione in modalità normale è la modalità operativa principale, in cui il dispositivo passa continuamente da periodi di accensione a periodi di spegnimento (ad esempio, 30 secondi di accensione e 5 minuti di spegnimento). La stimolazione in modalità magnetica consente al paziente o all’operatore di fornire una stimolazione su richiesta, attivata passando un magnete sull’area del generatore di impulsi impiantato (ciò si basa sul fatto che l’82% dei pazienti affetti da epilessia constatino un rapido aumento della frequenza cardiaca in concomitanza di una crisi e possano quindi “prevederla”). Il sistema di programmazione esterno consente di programmare i parametri di stimolazione, come l’intensità della corrente, misurata in milliampere (mA), e il ciclo di stimolazione, ovvero l’alternanza di periodi di accensione (ON Time) e spegnimento (OFF Time) nel corso della giornata.
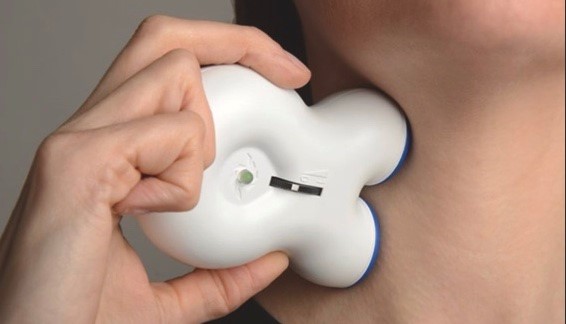
Ad oggi sono disponibili anche dispositivi più maneggevoli, ovvero sistemi che consentono la stimolazione esterna senza necessità di intervento chirurgico. Un esempio è rappresentato dalla stimolazione transcutanea del nervo vago (t-VNS). Attualmente, i principali dispositivi utilizzati sono due:
- n-VNS (electroCore LLC, Basking Ridge, NJ, USA) che stimola il nervo vago nel suo decorso cervicale (Fig. 3).
- t-VNS (Cerbomed, Erlangen, Germania) che stimola il ramo auricolare del nervo vago tramite un elettrodo bipolare attaccato alla pelle della conca auricolare.
Questi dispositivi presentano il vantaggio di non richiedere un impianto chirurgico né un intervento successivo per la sostituzione della batteria (solitamente necessario a distanza di circa cinque anni), rendendoli una soluzione meno invasiva e più pratica.
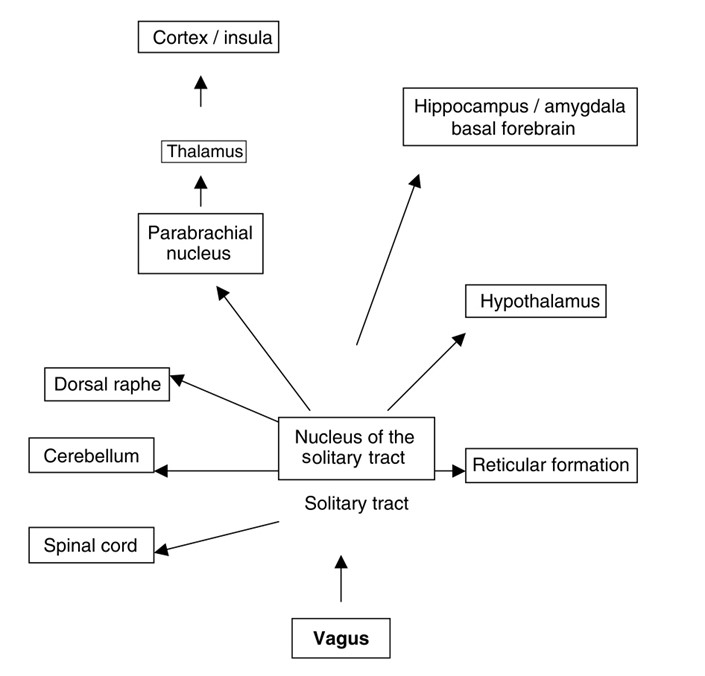
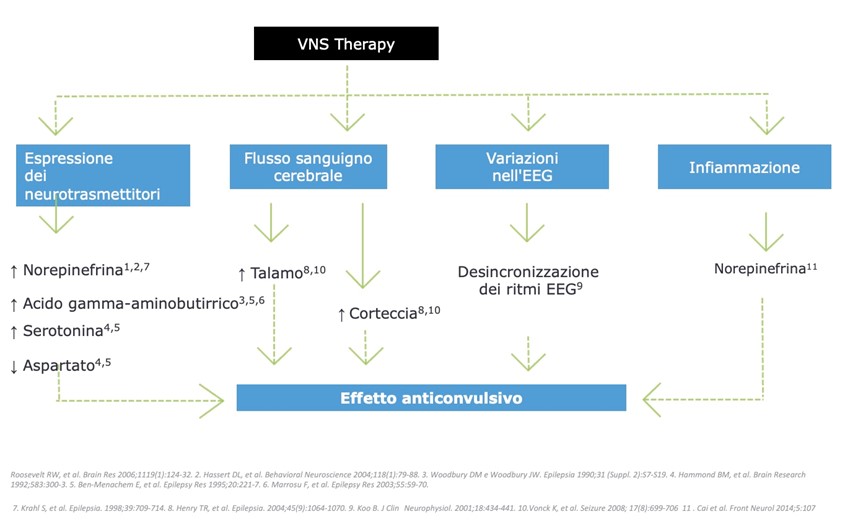
L’esatto meccanismo d’azione con cui la stimolazione del nervo vago (VNS) sopprime le crisi epilettiche non è ancora del tutto noto, ma in base agli studi sui modelli animali, si è ipotizzato che un’alta sincronizzazione dei circuiti corticali e talamocorticali sia alla base delle crisi stesse. Gli stimoli elettrici applicati al nervo vago, dunque, sono stati pensati per influenzare lo stato di eccitabilità cerebrale. Questo effetto è veicolato dal nervo vago stesso, che è composto per circa l’80% da fibre nervose afferenti. I loro corpi cellulari sono localizzati nel ganglio nodoso e proiettano principalmente verso il nucleo del tratto solitario (NTS). Gli input del nervo vago modulano le proiezioni verso questo nucleo. Le connessioni anatomiche estese del NTS nel sistema nervoso centrale potrebbero essere alla base dell’ampio effetto della VNS. I neuroni di questo nucleo, infatti, estendono le loro proiezioni a molteplici aree del prosencefalo e del tronco encefalico, e indirettamente al locus coeruleus e alla corteccia cerebrale attraverso connessioni diffuse. Tra le strutture rilevanti che si pensa possano mediare gli effetti antiepilettici e che ricevono input dal NTS figurano l’amigdala e il talamo. In aggiunta, le vie efferenti si estendono alla formazione reticolare, al prosencefalo basale, all’amigdala, all’ippocampo, all’ipotalamo, al rafe dorsale, al cervelletto e al midollo spinale. Il VNS ridurrebbe l’ipersincronizzazione grazie alle proiezioni del NTS ai nuclei del rafe e al locus coeruleus, aumentando la trasmissione serotoninergica e noradrenergica, come evidenziato dall’aumento dei livelli di serotonina, noradrenalina e dei suoi metaboliti nel liquido cerebrospinale dei pazienti sottoposti a stimolazione VNS.
Il VNS ha dimostrato la sua efficacia anche nelle cosiddette “popolazioni speciali”. Nelle donne in gravidanza, per esempio, sono riportati pochi dati in letteratura ma positivi. Secondo una review del 2021 (4), la stimolazione del nervo vago (VNS) sembra essere relativamente sicura ed efficace per la madre e il feto durante la gravidanza, e potrebbe non rendersi necessaria la sua disattivazione; ciò considerando che le donne in gravidanza con epilessia refrattaria presentano un rischio aumentato di complicanze ostetriche, tra cui iperemesi gravidica, parto prematuro, ipertensione gestazionale, preeclampsia, parto cesareo, distacco di placenta e mortalità perinatale. L’uso di farmaci anticrisi in particolare in regime di politerapia, è inoltre associato a un rischio maggiore di malformazioni fetali ed effetti cognitivi avversi a lungo termine sul bambino.
In conclusione, è importante comprendere, nella gestione delle epilessie farmacoresistenti, che la terapia con VNS non è risolutiva; solo il 20% circa di pazienti assiste a una riduzione > 90% delle crisi, e l’8% in media non ne ha più alcuna. Tuttavia, nella maggioranza dei casi (~70%) le crisi si riducono del 50% o più. Esse, tra l’altro, possono durare meno ed essere meno gravi; infine, molti pazienti hanno una ripresa più rapida dalle crisi stesse. Alcuni vantaggi aggiuntivi della terapia con VNS sono: l’assenza di un periodo “honeymoon”, l’aumento dell’efficacia nel tempo e la riduzione dell’incidenza e della gravità dello stato epilettico. Uno dei risvolti interessanti della VNS è, inoltre, il suo impatto sulle comorbidità psichiatriche nei pazienti epilettici, considerata l’indicazione all’impianto anche nel disturbo depressivo. In quest’ottica, dunque, questa metodica di stimolazione può realmente risultare life-changing per i pazienti che sperimentano un elevato numero giornaliero di crisi epilettiche e con comorbidità psichiatrica.
Bibliografia
- Fattorusso A, Matricardi S, Mencaroni E, Dell’Isola GB, Di Cara G, Striano P, Verrotti A. The Pharmacoresistant Epilepsy: An Overview on Existant and New Emerging Therapies. Front Neurol. 2021 Jun 22;12:674483. doi: 10.3389/fneur.2021.674483. PMID: 34239494; PMCID: PMC8258148.
- Kwan P, Arzimanoglou A, Berg AT, Brodie MJ, Allen Hauser W, Mathern G, Moshé SL, Perucca E, Wiebe S, French J. Definition of drug resistant epilepsy: consensus proposal by the ad hoc Task Force of the ILAE Commission on Therapeutic Strategies. Epilepsia. 2010 Jun;51(6):1069-77. doi: 10.1111/j.1528-1167.2009.02397.x. Epub 2009 Nov 3. Erratum in: Epilepsia. 2010 Sep;51(9):1922. PMID: 19889013.
- Toffa DH, Touma L, El Meskine T, Bouthillier A, Nguyen DK. Learnings from 30 years of reported efficacy and safety of vagus nerve stimulation (VNS) for epilepsy treatment: A critical review. Seizure. 2020 Dec;83:104-123. doi: 10.1016/j.seizure.2020.09.027. Epub 2020 Oct 10. PMID: 33120323.
- Jiangwei Ding, Lei Wang, Chaofan Wang, Caibin Gao, Feng Wang, Tao Sun, Is vagal-nerve stimulation safe during pregnancy? A mini review, Epilepsy Research, Volume 174,2021, 106671, ISSN 0920-1211, https://doi.org/10.1016/j.eplepsyres.2021.106671
Chiara Martellino
Università degli studi di Messina
chiamart10@gmail.com
Giorgia Atanasio
Università degli studi di Messina
Giorgia_Atanasio@outlook.it