Le atrofie muscolari spinali (SMA) sono un gruppo di malattie neuromuscolari ereditarie, autosomiche recessive, che colpiscono entrambi i sessi e caratterizzate da una degenerazione progressiva dei motoneuroni alfa delle corna anteriori del midollo spinale, con incidenza di circa 1 su 10 mila nati vivi (in Italia ogni anno nascono circa 40–50 bambini affetti mentre in Europa si stima intorno ai 600). Le forme a trasmissione autosomica recessiva sono state distinte in 3 tipi sulla base del fenotipo clinico:
- Tipo 1, la forma più grave e interessa circa il 50% dei pazienti, con ipotonia e ipostenia generalizzata già presente alla nascita o nei primi mesi di vita e con impossibilità di raggiungere la stazione eretta autonomamente. La prognosi è molto grave, con morte in genere entro il primo anno di vita nell’80% dei casi per insufficienza respiratoria. L’ipotonia interessa soprattutto i muscoli del cingolo pelvico e dei distretti prossimali e la respirazione è diaframmatica, con ipotrofia dei muscoli accessori e torace a campana
- Tipo 2, forma intermedia che esordisce intorno al sesto mese, e dove i bambini arrivano in genere al controllo del capo e alla posizione seduta ma non sono in grado di alzarsi autonomamente può esservi tremore alle mani e fascicolazioni.
- Tipo 3, esordisce dopo i primi anni di vita con ipostenia prossimale simmetrica e lentamente ingravescente, iperlordosi lombare compensatoria e difficoltà nei passaggi posturali (manovra di Gowers positiva). L’evoluzione della ipostenia è in genere lenta e la prognosi è favorevole per quanto riguarda la durata della vita.
Studi di biologia molecolare hanno mappato il locus della SMA sul cromosoma 5 (5q1.1-13.3). Una piccola delezione trovata in pazienti affetti ha permesso di identificare la porzione telomerica del gene SMN (noto come SMN 1) come porzione condizionante la patologia: la SMA è quindi causata da una mutazione del gene SMN1, che si trova sul cromosoma 5 e che codifica per una proteina fondamentale per il trofismo e la sopravvivenza dei motoneuroni chiamata proteina SMN (Survival Motor Neuron). Nella SMA questa proteina viene prodotta in quantità insufficiente e questo causa la degenerazione dei motoneuroni.
Essendo una malattia autosomica recessiva, Per essere affetti clinicamente, un individuo deve ereditare due alleli SMN1 difettosi, uno da ciascun genitore (Questo è spesso indicato come 5q- riferendosi alla localizzazione del gene sul cromosoma 5, nel braccio lungo q). I genitori di un individuo affetto possono essere portatori malati (con 2 alleli SMN1 difettosi), oppure possono avere solo un allele SMN1 non funzionante, e quindi non esprimere il fenotipo di malattia (status di portatore). Questa è la situazione più comune e si stima che circa 1 su 50 persone in tutto il mondo sono portatrici sane della SMA. Per ogni gravidanza c’è una probabilità del 25% di avere un figlio affetto, il 50% di avere un figlio portatore sano e il 25% di avere un figlio che non ne è affetto e non è portatore. Il 95% dei pazienti affetti presenta una delezione in omozigosi sia dell’esone 7 che dell’8 del gene SMN1 che produce un trascritto contenente 9 esoni. Nel genoma umano tuttavia sono presenti due forme del gene codificante per la proteina SMN :SMN 1, che genera un mRNA tradotto nella proteina completamente funzionante, e SMN 2, presente a livello centromerico e che differisce dal precedente per un solo nucleotide nell’esone 7 e, a causa dello splicing, origina un trascritto più corto del precedente che viene rapidamente degradato. Nel 10% dei trascritti di SMN 2 però lo splicing alternativo causa l’inclusione dell’esone 7 originando un peptide funzionalmente attivo. Recenti studi mostrano come vi è una forte correlazione inversa tra il numero delle copie di SMN 2 e l’attività di malattia.
Fino a pochi anni fa non esistevano terapie proponibili per questi pazienti, destinati all’exitus o ad accumulo di grave disabilità neuromotoria. Le cose sono cambiate a partire dall’immissione in commercio di un farmaco orfano, il nusinersen ( SPINRAZA) nel 2017. Si tratta di un oligonucleotide antisenso (una corta molecola di acido ribonucleico) somministrato in forma di soluzione iniettabile da 12 milligrammi, soggetto ad uso esclusivo ospedaliero (fascia H) con prescrizione limitativa e destinato a pazienti di qualunque età affetti da SMA 5q e dove I dati degli studi clinici hanno evidenziato risultati significativi in termini di aumento della sopravvivenza nei bambini affetti dalla malattia e di raggiungimento di importanti tappe motorie dello sviluppo (controllo della testa, della posizione seduta, il gattonamento ed il cammino).
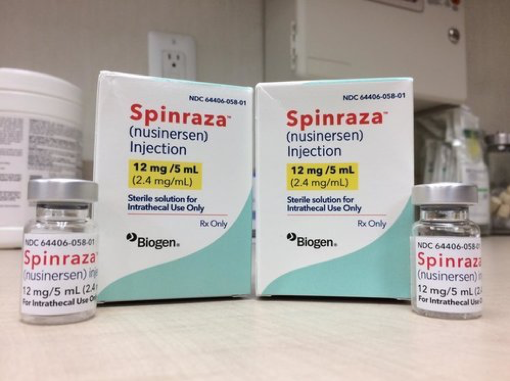
Nusinersen è un oligonucleotide antisenso (ASO) 2’-O- metossietilenico di sintesi chimica (in cui i gruppi 2’-idrossi degli anelli ribofuranosilici sono sostituiti con gruppi 2’-O-2-metossietilici e i gruppi fosfato sono sostituiti con fosforotioato), un polimero di alto peso molecolare costituito da nucleotidi che agisce da modulatore dell’espressione genica, legando uno specifico RNA bersaglio tramite complementarietà delle basi azotate per indurre il gene SMN2 a produrre il “fattore di sopravvivenza dei motoneuroni” funzionante, a lunghezza completa, attivandone la funzione (tramite ingombro sterico impedisce lo splicing dell’esone 7). Questo gene, essendo complementare a quello inattivo nella malattia (SMN1), determina la sintesi della stessa proteina carente nelle cellule nervose e sostituisce la proteina non prodotta da SMN1, alleviando così i sintomi della SMA. Viene somministrato per via intratecale mediante un ago per puntura lombare, in bolo in pochi minuti, con 4 dosi di carico ai Giorni 0, 14, 28 e 63 e successivamente una dose di mantenimento una volta ogni 4 mesi. La necessità di continuare la terapia deve essere verificata periodicamente e considerata su base individuale, in funzione del quadro clinico e della risposta alla terapia del paziente. Nusinersen viene metabolizzato lentamente attraverso idrolisi mediata da esonucleasi (3’ e 5’) e non dal CYP450, di cui non è induttore ne inibitore. L’emivita media nel LCS è 135-177 giorni e la via di eliminazione principale è quella renale. Lo studio ENDEAR ha coinvolto 121 neonati (età media 7 mesi) con SMA per valutare nusinersen rispetto al placebo. Dopo un anno di trattamento, in 37 neonati dei 73 trattati con nusinersen (51%) sono stati osservati progressi nell’attività motoria, in particolare miglioramenti nel:
- controllo del capo,
- rotolarsi,
- mantenere la posizione seduta,
- gattonare,
- alzarsi in piedi,
- camminare.
Nel gruppo di controllo con placebo, invece, non è stato osservato alcun progresso. Inoltre, la maggior parte dei neonati cui è stato somministrato nusinersen è sopravvissuta più a lungo. Anche la necessità di ricorrere a respirazione assistita è stata ritardata. Un altro studio (CHERISH)ha valutato l’efficacia di nusinersen in bambini con SMA meno grave, diagnosticata a un’età media 3 anni. In questo studio, dopo 15 mesi di trattamento, nel 57% dei bambini trattati con nusinersen ha mostrato un miglioramento nel movimento vs il 26% dei bambini che avevano ricevuto placebo. Nusinersen è un farmaco biotecnologicamente avanzato ma, come tutti gli ASO, NON rientra tra gli ATMP e quindi non è considerato come terapia genica.
Di recente, nel 2019, è stato invece approvato un altro farmaco, Onasemnogene abeparvovec (ZOLGENSMA), che rientra nell’ambito della terapia genica.
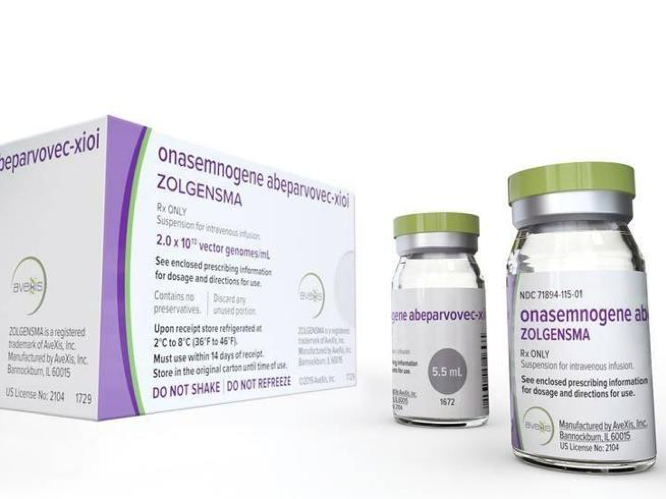
Si tratta di un farmaco ospedaliero in soluzione iniettabile per uso endovenoso indicato (e rimborsato dal SSN) per il trattamento della SMA 5q in pazienti con peso corporeo fino a 13,5 kg: diagnosi clinica di SMA di tipo 1 ed esordio nei primi sei mesi di vita, oppure diagnosi genetica di SMA di tipo 1 (mutazione biallelica nel gene SMN1 e fino a due copie del gene SMN2).
E’ prodotto su cellule di rene embrionale umano mediante tecnologia del DNA ricombinante ed è costituito da un vettore virale adeno-associato di sierotipo 9 (AAV9) ricombinante, incapace di replicare in vivo, contenente il cDNA per il gene umano SMN. Ogni millilitro contiene una concentrazione nominale di 2 × 10^13 genomi vettoriali (vg). Il quantitativo di farmaco da utilizzare viene valutato in base al peso corporeo; il trattamento viene effettuato una sola volta nella vita (sia perché il costo del farmaco è elevatissimo, circa un milione e 500 mila euro per flaconcino,( mentre il prezzo del nusinersen è intorno ai 115 mila euro), sia perché la somministrazione in vivo genera un titolo anticorpale contro il vettore ed eccipienti che impedirebbe ulteriori benefici per successive iniezioni) ed I pazienti ricevono una dose di 1,1 x 10^14 vg/kg di farmaco per via endovenosa lenta in circa un’ora.
Onasemnogene abeparvovec è progettato per introdurre una copia funzionale del gene SMN1 nelle cellule trasdotte al fine di intervenire sulla causa all’origine della malattia, fornendo una fonte alternativa di espressione della proteina SMN nei motoneuroni. Si tratta di un vettore AAV ricombinante, non-replicante che usa un capside AAV9 per veicolare un transgene SMN umano stabile, pienamente funzionante. Il capside di AAV9 ha dimostrato la capacità di attraversare la barriera ematoencefalica e di trasdurre i motoneuroni. Il gene SMN1 presente nel farmaco è progettato per risiedere, sotto forma di DNA episomiale, nel nucleo delle cellule trasdotte e si prevede una sua espressione stabile per un periodo di tempo esteso nelle cellule post-mitotiche. Il transgene viene introdotto nelle cellule bersaglio come molecola a doppio filamento, autocomplementare. La sua espressione è indotta da un promotore costitutivo che determina l’espressione continua e sostenuta delle proteine SMN. Dopo la somministrazione si verifica una risposta immunitaria al capside del vettore virale e ciò può portare ad aumenti delle transaminasi epatiche, della troponina I o riduzioni delle conte piastriniche. Per attenuare la risposta immunitaria, si può attuare l’immunomodulazione con corticosteroidi (prednisolone orale), partendo da 24 ore prima del trattamento e proseguendo per un mese. Onasemnogene abeparvovec è risultato rilevabile in vari campioni biologici dopo infusione: La clearance avviene principalmente per via fecale e la maggior parte viene eliminata entro 30 giorni dalla somministrazione della dose. La biodistribuzione è stata valutata in 2 pazienti deceduti rispettivamente a 5,7 mesi e 1,7 mesi dopo l’infusione alla dose di 1,1 x 10^14 vg/kg ed entrambi ì hanno evidenziato che livelli massimi di DNA vettoriale sono stati rilevati nel fegato. Il DNA vettoriale è stato rilevato anche nella milza, nel cuore, nel pancreas, nel linfonodo inguinale, nei muscoli scheletrici, nei nervi periferici, nei reni, nei polmoni, nell’intestino, nel midollo spinale, nel cervello e nel timo. L’immunoistochimica per la proteina SMN ha evidenziato un’espressione generalizzata di SMN nei motoneuroni spinali, nelle cellule neuronali e gliali del cervello, e nel cuore, nel fegato, nei muscoli scheletrici e in altri tessuti valutati. In base ad alcuni recenti studi, come quello di fase 3 SPRINT, i bambini trattati pre-sintomaticamente con onasemnogene abeparvovec nel corso dello studio di hanno raggiunto traguardi motori appropriati all’età rientranti nei parametri di normale sviluppo, ivi inclusa la capacità di stare seduti o in piedi, e quella di camminare, erano in grado di alimentarsi esclusivamente per bocca e non hanno avuto bisogno di alcun supporto ventilatorio. Durante lo studio clinico SPR1NT non sono stati segnalati eventi avversi gravi correlati al trattamento. I dati di follow-up a lungo termine di due studi hanno continuato a dimostrare che i bambini trattati con onasemnogene abeparvovec hanno sperimentato un beneficio prolungato della terapia genica anche negli anni successivi alla somministrazione, senza alcuna evidenza di segnali di sicurezza, nuovi o ritardati. Anche a distanza di anni dal trattamento, onasemnogene abeparvovec ha permesso di raggiungere nuovi traguardi, inclusa la capacità di rimanere seduti, con una durabilità prolungata nei bambini ora fino a sei anni di età e oltre cinque anni dopo il trattamento. Quasi tutti i bambini con due o più valutazioni basate sulla scala CHOP INTEND, per la misurazione della funzionalità motoria in pazienti con patologie neuromuscolari, hanno migliorato o mantenuto i propri punteggi, e la maggior parte ha mostrato un aumento clinicamente significativo, pari o superiore a 4 punti.
In conclusione possiamo affermare che, pur essendo entrambi medicinali avanzati e indicati per il trattamento della SMA, le principali differenze tra spinraza e zolgensma riguardano la modalità di somministrazione (intratecale vs endovenosa), la posologia (somministrazione ripetuta vs singola), la tipologia di pazienti (Zolgensma è solo per SMA di tipo 1 e in pazienti pediatrici), il costo, la tipologia di prodotto (Zolgensma è un ATMP vettore-associato mentre spinraza è un ASO).
In entrambi i casi si è riusciti ad ottenere un significativo miglioramento delle performance motorie e rallentamento del decorso di malattia per i Pazienti candidati al trattamento; resta ancora da sciogliere il nodo relativo al prezzo ed ai criteri di rimborsabilità per zolgensma per esatendere la sua prescrivibilità, cosi come la valutazione a lungo termine della farmacovigilanza relativa a questi farmaci ancora innovativi.
BIBLIOGRAFIA E SITOGRAFIA
- Ruggieri M, franzoni E. Neurologia e psichiatria dello sviluppo. Elsevier, 2012
- Ruggieri M, Pavone L. Neurologia pediatrica. Elsevier, 2015
- Vegeto E, maggi A. farmaci biotecnologici aspetti farmacologici e clinici. Zanichelli, 2020
- Militerni R. Neuropsichiatria infantile settima edizione, idelson-gnocchi, 2021
- https://www.ema.europa.eu/en/documents/product-information/zolgensma-epar-product-information_it.pdf
- https://www.ema.europa.eu/en/documents/product-information/spinraza-epar-product-information_it.pdf
- https://www.osservatoriomalattierare.it/malattie-rare/sma-atrofia-muscolare-spinale/17198-sma-nuove-evidenze-confermano-l-efficacia-della-terapia-genica
- https://www.osservatorioterapieavanzate.it/terapie-avanzate/terapia-genica
MAROVINO EDOARDO (Università scienze del farmaco, Pavia)